【材料】メディシノバ---米学会でMN-166のALS(筋萎縮性側索硬化症)を適応とする臨床治験での追加臨床データ発表
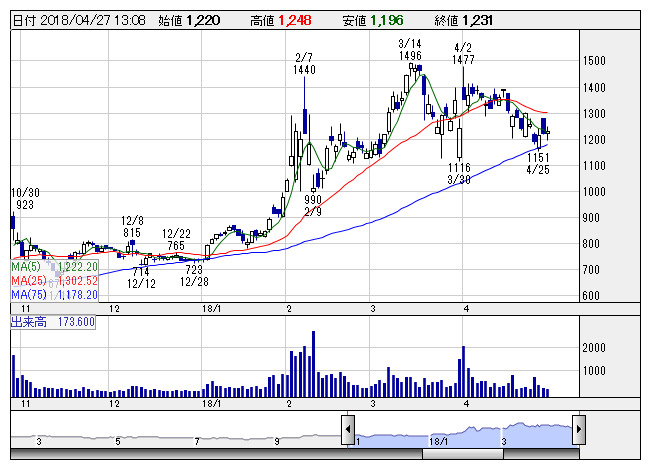 メディシノバ <日足> 「株探」多機能チャートより
メディシノバ <日足> 「株探」多機能チャートよりメディシノバ<4875>は、現地時間2018年4月27日にロサンゼルスで開催中の米国神経学会第70回年次総会において、主任治験医師がMN-166のALS(筋萎縮側性索硬化症)を適応とする臨床治験の追加臨床データを発表する。
治療反応者の比率はMN-166(イブジラスト)群が32.4%およびプラセボ群が11.8%と、MN-166(イブジラスト)群は、プラセボ群と比較し高かった。 また、治療反応者は、MN-166(イブジラスト)治療後30ヶ月における生命表法生存率が有意に改善された。 加えて、治験完遂者、6ヶ月または12ヶ月のMN-166(イブジラスト)治療を完遂した患者は治療後30ヶ月における生命表法生存率が有意に改善されたという。
本治験主任責任医師であるベンジャミン・リックス・ブルックス博士は次のようにコメントしている。
「この複合エンドポイント解析結果は、ALS患者の一部の人にイブジラストが疾患の進行を遅らせ、さらに生存率へ寄与する可能性を示しています。治療反応者の比率は、二重盲検期間のイブジラスト群では、 約1/3(11/34)でプラセボ群より高かった。この治療反応者の比率は、PRO-ACTデータベースの 何千人ものALS患者の疾病自然史(訳注:疾病自然史とは何ら医学的処置を加えない状態での疾病の自然経過のこと)や、現在受けることができるALS治療と比べて大きいものです。 この新たな複合臨床エンドポイントは、ALS適応において、イブジラストや他の治療法での、将来のフェーズ2およびフェーズ3臨床治験において有用と考えます。」
また、代表取締役社長兼CEOの岩城氏は次のようにコメントしている。
「今回の新たな解析結果から、MN-166がこの深刻で致命的な疾病の生存率を改善する可能性があることを非常に嬉しく思っています。この研究のポジティブな結果を受け、米国食品医薬品局(FDA)と開発計画の次のステップについて話し合う予定です。」
なお、本件が2018年12月期の業績に与える影響は現在のところ未定だが、業績に重要な影響を及ぼすことが明らかになった場合、確定次第速やかに発表するとのこと。
《TN》
提供:フィスコ

 米株
米株










